Polícia agora só pode prender em flagrante
24 de outubro de 2022
Valmir virou o patinho feio da campanha
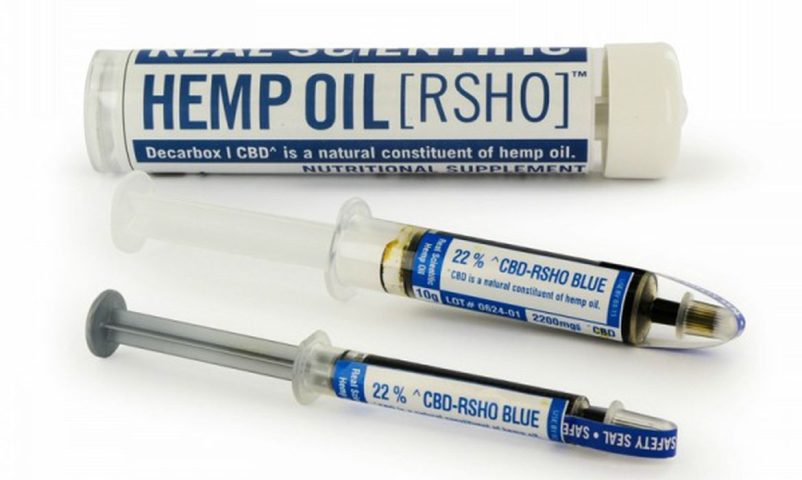
24 de outubro de 2022Saiba os prós e contras do uso da maconha medicinal
A discussão sobre Cannabis medicinal e psiquiatria tem várias impropriedades. Quem pensa assim é o médico Marcelo Allevato, filiado à Associação Brasileira de Psiquiatria. No caso da doença de Alzheimer, que é a forma mais comum de demência neurodegenerativa em pessoas de idade, por exemplo, Allevato descartou que haja relação com a Cannabis medicinal. “É uma demência, e a Cannabis não tem possibilidade nenhuma de tratar demência. Pode tratar, teoricamente, algumas alterações de comportamento, mas não tem nenhuma evidência consistente disso ainda não. É só uma possibilidade.”
Segundo Allevato, existem muitas impropriedades sobre “medicamentos” à base de Cannabis. Ele disse que, de acordo com a Agência Nacional de Vigilância Sanitária (Anvisa), existe apenas um medicamento à base de Cannabis, mas destacou que há produtos à base da planta, que são registrados com autorização provisória, com duração de cinco anos, que podem ser usados quando se esgotam todas as possibilidades terapêuticas disponíveis no mercado brasileiro.
Desenvolvido em várias fases, da concepção da ideia até os testes clínicos, e depois comercializado, o único medicamento à base de Cannabis existente no Brasil é o Mevatyl, liberado como adjuvante no tratamento de espasticidade na esclerose múltipla, causada por danos ou lesões na parte do sistema nervoso central (cérebro ou medula espinhal) que controla o movimento voluntário. “Este é o único medicamento à base de Cannabis existente no Brasil. Chamar produto à base de Cannabis de medicamento é uma impropriedade”, reiterou o médico.
Confirmação
Segundo a Anvisa, até o momento, o único medicamento à base de Cannabis registrado no Brasil tem o nome comercial de Mevatyl. De acordo com a Agência, o Mevaty é um medicamento, pois passou pelos mesmos requisitos técnicos aplicados a todos os demais registrados na agência, o que envolve estudos clínicos e comprovação de segurança e eficácia, entre outras exigências. O Mevatyl foi registrado em 9 de janeiro de 2017 com indicação no tratamento sintomático da espasticidade moderada a grave relacionada à esclerose múltipla.
Os demais itens regularizados pela Anvisa são categorizados tecnicamente como produtos derivados de Cannabis, um segmento específico criado em 2019 (Resolução RDC 327), que não tem indicação terapêutica específica e cuja análise de benefício deve ser feita pelo médico, de acordo com o caso de cada paciente.
Ainda de acordo com a Anvisa, os produtos derivados de Cannabis recebem autorização sanitária, e não registro, para que possam estar à disposição dos pacientes. “Ou seja, a indicação e a forma de uso dos produtos derivados de Cannabis são de responsabilidade do médico que assiste o paciente, que faz tal indicação a partir da avaliação de que seu paciente pode se beneficiar do tratamento, especialmente em casos para os quais não há opções terapêuticas disponíveis”.
Sem liberação
Allevato afirmou que não há, em lugar algum do mundo, medicamento à base de Cannabis liberado para uso psiquiátrico. Legislações de alguns países permitem o uso de derivados da Cannabis em situações excepcionais, em algumas enfermidades. Isso ocorre, por exemplo, em Israel e na maioria dos estados norte-americanos. “Mas tudo dentro de um controle muito rígido, após se esgotarem as possibilidades terapêuticas”.
O médico disse que, no Brasil, o que houve foi uma “tentativa de disseminar um uso que é completamente contrário ao que é preconizado. Na verdade, é disseminar um uso de maneira indiscriminada, ou seja, tenho ansiedade, vou tomar canabidiol”. O mesmo se aplica para depressão, insônia, Alzheimer, autismo. O médico sustentou que não há evidência científica sólida para isso. Ele admitiu, porém, que, em casos em que o paciente não responde a nada, o médico pode usar esses produtos. É o chamado uso compassivo.
Fonte e foto: Agência Brasil